
Препарат КСОФИГО® ПРЕДНАЗНАЧЕН для лечения пациентов с кастрационно-резистентным раком предстательной железы, c наличием костных и отсутствием висцеральных метастазов.
Для специалистов здравоохранения
КЛИНИЧЕСКИЕ ИСХОДЫ ПРИМЕНЕНИЯ ПРЕПАРАТА КСОФИГО® У ПАЦИЕНТОВ С мКРРПЖ ЗАРЕГИСТРИРОВАНЫ В ЧЕТЫРЕХ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ, ПРОВЕДЕННЫХ В УСЛОВИЯХ РЕАЛЬНОЙ КЛИНИЧЕСКОЙ ПРАКТИКИ.
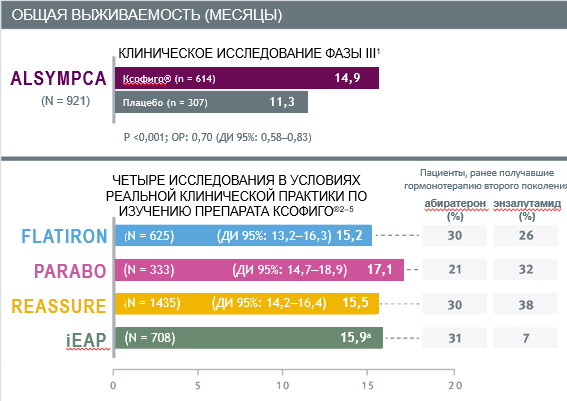
Зарегистрировать радий-223 для лечения КРРПЖ с метастазами в кости позволило исследование III фазы ALSYMPCA. В нем участвовали пациенты с костными метастазами, но без висцеральных метастазов. Больные получали радий-223 в дозировке 50 кБк/кг 1 раз в 4 недели, было запланировано максимально 6 введений. У пациентов с КРРПЖ с метастазами в кости в 1-й линии терапии и после доцетаксела радий-223 показал достоверное преимущество ОВ на 3,6 месяца, увеличение времени до первого костного осложнения на 5,8 месяца. Преимущество ОВ было особенно выражено у пациентов, получивших 5 и более инъекций радия-223. Медиана ОВ составила 17,9 месяца, а у пациентов, которые получили менее 5 введений, медиана выживаемости существенно ниже — только 6,2 месяца. В связи с чем, рекомендуется проведение минимум 5-6 инъекций для достижения максимального эффекта от терапии радием-223.
Для получения дополнительной информации об эффективности и безопасности, а также для лучшего понимания места препарата радия-223 в парадигме лечения пациентов с мКРРПЖ были инициированы ряд исследований в реальной клинической практике.
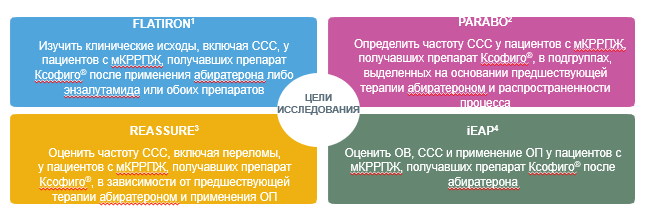
Эффективность и безопасность Ra-223 была подтверждена в широкой клинической практике.
Один из этих протоколов iEAP – это 696 больных, получивших в реальной клинической практике препарат Ксофиго® (радий-223) в стандартном режиме. Отличие группы больных в этом наблюдательном исследовании от исследования ALSYMPCA в том, что в нее включались пациенты с бессимптомным течением КРРПЖ (20%). Больные могли получать до радия-223 не только доцетаксел, но и препараты с антиандрогенной активностью — абиратерон и энзалутамид. Медиана ОВ оказалась не ниже, а даже несколько выше по сравнению с исследованием ALSYMPCA (15,9 месяцев и 14,9). Медиана времени до роста щелочной фосфатазы (ЩФ) составила 8 месяцев.
REASSURE – международное обсервационное исследование применения радия-223 у больных мКРРПЖ. Основные конечные точки – не только супрессия костного мозга и профиль безопасности при кратковременном и длительном применении радия-223, но и частота выявления вторичного онкологического процесса. По безопасности применения радия-223 НЯ оценены у 1465 больных. При этом меньше, чем у половины (48%) больных наблюдались любые НЯ, но 3-я степень выявлена только у 11% пациентов, а побочные эффекты, которые привели к отмене лечения радием-223, зарегистрированы лишь у 6% пациентов. Из всех НЯ выявлены только диарея (11%), тошнота (9%) и анемия (8%) – ни нейтропении, ни тромбоцитопении в лидирующих позициях не было. Опираясь на полученные данные, можно сделать вывод, что радий-223 первый радиофармпрепарат, обладающий такой низкой гематологической токсичностью. Медиана ОВ в этом наблюдательном исследовании составила 15,5 месяца, то есть не хуже, а даже несколько выше, чем в исследовании ALSYMPCA. Только у 14 больных (1%) выявлены вторичные опухолевые очаги, при этом 71% (10 из 14) ранее получали дистанционную лучевую терапию, поэтому возможная причина развития этих опухолей – именно ДЛТ, не радионуклидная терапия.
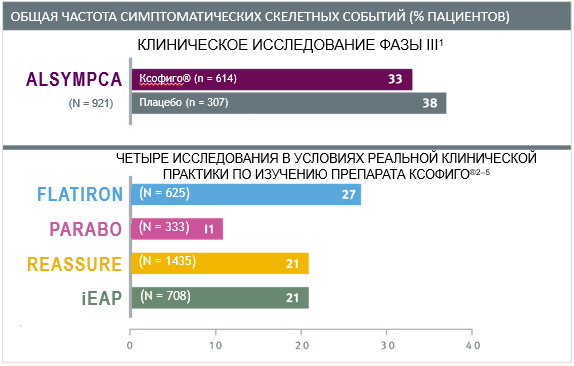
Анализ базы данных FLATIRON - протокол включил 625 пациентов, которые получали радий-223 с 2013 по 2017 годы. Помимо выживаемости оценивали прежде всего частоту симптоматических скелетных событий. В рамках протокола FLATIRON пациенты могли получать гормональные препараты абиратерон и энзалутамид до, после или даже одновременно с радием-223. У пациентов, которые получали сопутствующие остеомодифицирующие препараты, частота возникновения патологических переломов была меньше. Показатель ОВ составил – 15,2 месяца, что сопоставимо и даже несколько выше, чем в рамках исследования ALSYMPCA. По данным регистра FLATIRON показано, что применение радия-223 возможно и последовательно с антиандрогенными препаратами, и даже в комбинации. И хотя подобная схема на сегодняшний день не зарегистрирована в РФ, но частота осложнений при последовательном или даже одномоментном применении радия-223 с абиратероном и энзалутамидом не увеличивается, а применение костно-модифицирующих агентов деносумаба или бисфосфонатов снижали частоту патологических переломов и других осложнений, связанных с метастатическим поражением скелета.
Так же стоит упомянуть продолжающееся проспективное наблюдательное исследование PARABO, в рамках которого пациенты с мКРРПЖ и костными метастазами, получают терапию препаратом Ксофиго® в условиях реальной клинической практики в Германии. Основной целью данного исследования является определение частоты симптоматических скелетных событий и уровень болевого синдрома у пациентов с мКРРПЖ, получавших препарат Ксофиго®. Подгруппы выделены на основании предшествующей терапии абиратероном в сочетании с преднизолоном и энзалутамидом, а также в зависимости от распространенности процесса. Результаты исследования ожидаются в 2023 году.
Таким образом, радий-223 подтвердил в реальной клинической практике результаты эффективности и безопасности, продемонстрированные в регистрационном исследовании ALSYMPCA, а в ряде протоколов результаты показателя общей выживаемости, симптоматических скелетных событий и частоты развития НЯ были ниже чем в рамках клинического исследования.
Список литературы:
- Higano C, Tombal Bet al. Clinical outcome with radium-223 in patients previously treated with abiraterone or enzalutamide: a retrospective study of real-world data from patients with metastatic castration-resistant prostate cancer. Poster no. 827P. Munich, Germany.
- Poeppel T, Eschmann S, et al. Symptomatic skeletal event dynamics in patients with metastatic castration-resistant prostate cancer treated with radium-223: an interim review of a prospective, non-interventional study (PARABO). Poster no. 828P. Munich, Germany.
- Sternberg CN, Tombal B, et al. Use of bone health agents in patients with metastatic castration-resistant prostate cancer treated with radium-223 after abiraterone: an interim review of REASSURE. Poster no. 826P.
- Miller K, Heinrich D, et al. Radium-223 therapy after abiraterone: analysis of symptomatic skeletal events in an international Early Access Program in patients with metastatic castration-resistant prostate cancer. Poster no. 824P.